Az endotoxin mérés alapjai
A múltban az endotoxin kimutatására
a "nyúl tesztet" alkalmazták. A nyulat beoltva
a vizsgálandó mintával, figyelték a
nyúl testhőmérsékletének változását.
Lázas reakció esetén a minta endotoxint tartalmazott.
Ennek a módszernek több hátránya is van.
Az anyagi és etikai kérdéseken túl a
módszer nagyon időigényes és nem kvantitatív.
Pontosabb mérések szükségessége
esetén a módszer érzékenysége,
pontossága és reprodukálhatósága sem kielégítő.
A parenterális készítmények
és gyógyászati eszközök pirogén-szennyezettsége
megállapításának legelterjedtebb módszere
a patkórákból kivont Limulus Amoebocyte Lysate-re
(LAL) alapozott mérés, mivel ez a
legérzékenyebb, reprodukálható és
gazdaságos eljárás, amellyel meghatározható
a Gram-negatív bakteriális eredetű endotoxin
(pirogén). Ez a rendkívül érzékeny
teszt kezdetben is különösen hasznosnak bizonyult
olyan termékek pirogén vizsgálatára,
amelyeket a nyulakon nehezen lehetett tesztelni (pl. intrathekális
injekciók, radioaktív gyógyszerek, rákgyógyászati
szerek és bizonyos biológiai készítmények).
A patkórák, tudományos nevén Limulus
polyphemus, közeli rokona a pókoknak. E különös
tengeri élőlény négy fajtája
élte túl az elmúlt 500 millió évet.
Jelenleg az USA keleti és Ázsia délkeleti partjainál
fordulnak elő legnagyobb számban.
A patkórák az óceánban él társközösségben
a Gram-negatív baktériumokkal. Az embertől
eltérően a keringési rendszere nyitott, ahol
a vér direkt kontaktusban áll a szövetekkel.
A páncélzat repedésén át bekerülő
baktériumok így pillanatok alatt eljuthatnak a szervezet
minden pontjához. (Az ember esetében több ezer
kilométer hosszú véredény rendszer szállítja
a vért a kapilláris hálózatokon keresztül
a szövetekhez.) Ezért a patkórák egy rendkívül szenzitív védelmi rendszert fejlesztett ki,
amely képes felismerni a baktériumok jelenlétét
a lipopoliszacharidjukon (LPS) keresztül. A védelmi
rendszer katonái a vérsejtek (amőbaciták).
Normális esetben ezek végzik a szokásos vérsejtekhez
kapcsolódó feladatokat (elnyelik az idegen vagy az
elpusztult sejteket, szállítják és tárolják
a megemésztett anyagokat, helyrehozzák a sérüléseket
stb.). Ezek a sejtek ovális alakúak és kis
szemcsékbe szerveződnek. Ezek a szemcsék tartalmazzák
az alvadási faktort (koaguláns), amit a baktérium
érzékelése esetén kibocsátanak
a környezetükbe. Ezek a koagulánsok, reakcióba
lépve az LPS-sel, nagyon rövid idő alatt
megalvasztják a környező folyadékot, ezáltal
csapdába ejtik a behatoló baktériumot. Ezek
a megalvadt részek annyira stabilak, hogy még a csapdába
ejtett baktérium Brown-féle mozgását
is megakadályozzák.
 A patkórákok ezen képességét
használják ki az endotoxin mérések kivitelezésekor.
A Limulus Amoebocyte Lysate (LAL) reagenst a patkórákok
véréből nyerik. A vérvétel után
a patkórákokat 24 órán belül visszaengedik
az óceánba, ahol teljesen felépülnek.
A vér a folyékony szérum és a szuszpendált
amőbaciták keveréke. Centrifugálással
a két összetevő elkülöníthető.
A cső alján összegyűlt pelletet átmossák,
szuszpendálják és összegyűjtik.
Az összegyűjtött vérsejteket desztillált
vízzel keverik, így a vérsejtek friss vizet
abszorbeálnak és híznak egészen addig,
amíg szét nem robbannak. A folyamat eredményeként
a koaguláns oldatba kerül. Az oldatot szűrik,
eltávolítják a sejttörmelékeket,
majd -80 °C -on szárítják. A folyamat végén
kinyert fehér porszerű anyag a LAL, amelyet az endotoxin
mérésekhez használnak, mint reagenst.
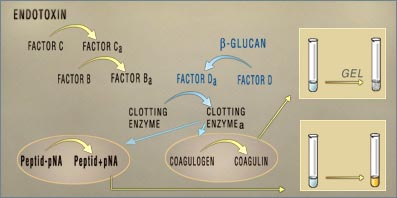
A LAL az endotoxinnal reakcióba lépve masszív
gélképződést, megnövekedett viszkozitást
és opaleszkálást vált ki. A koagulációs
folyamatot az endotoxin hatására fellépő
reakciók láncolata építi fel. Ez a több
lépéses reakció teszi rendkívül
érzékennyé a LAL rendszert, hiszen egymást
erősítő folyamatok láncolatából
áll.
A mintában lévő endotoxin mennyiségi
meghatározására a gél-képződésen
és a színreakción alapuló LAL-méréseket
használják. Mindkét esetben lehetőség
van végpontos és kinetikus mérésre
is.
A gél-képződésen alapuló mérés
mechanizmusa egy endotoxin által indukált katalitikus
folyamat, amelyben az aktivált enzim (koaguláz) specifikus
kötéseket hidrolizál a koagulogén fehérjében.
A hidrolizált kötéseket tartalmazó koagulin
fehérjék összekapcsolódnak és gélformában
kialakuló alvadékot képeznek. Az aktiváció
kezdeti sebességét az endotoxin koncentrációja
határozza meg.
- A kvantitatív színreakción alapuló
meghatározás során egy endotoxin által
aktivált enzim para-nitroanilint (pNA) szabadít fel egy
színtelen, szintetikus szubsztrátból (Ac-Ile-Glu-Ala-Arg-pNA),
sárga elszíneződés kíséretében.
A pNA kiválást fotometriásan 405 nm-en mérik.
A színintenzitás és az endotoxin-koncentráció
közötti korreláció, kinetikus méréstechnika
alkalmazása esetén a 0,005-50,0 EU/ml tartományban
lineáris (végpontos technika esetén ez az érték
0,01-1,0 EU/ml).
 A LAL méréseket a cégünk által kifejlesztett,
korszerű, megbízható és validált
eszközökkel valamint a PyroSolution program segítségével végezhetjük el.
A mérésekhez alkalmazott folyamat rövid leírása:
- endotoxin standard sor előállítása
- a minták előkészítése
- a mikrolemez feltöltése
- a mérőprogram és a fotométer konfigurálása
- a mikrolemez-kinetikus mérés elindítása
- a nyers adatok kvalifikálása
- az eredmények kiértékelése
- a riportok nyomtatása
- az eredmények jóváhagyása
- archiválás
- az eredmények kiküldése
Ez az eljárás - és a hozzátartozó
metodika - megfelel az európai és az amerikai gyógyszerhatóságok
előírásainak és a WHO követelményeinek.
A LAL mérések felhasználási területei:
- hemodialízisben használt oldatok vizsgálata
- orvosi segédeszközök vizsgálata
- infúziós oldatok vizsgálata
- injekciók vizsgálata
- táptalaj vizsgálata
- vérkészítmények vizsgálata
- biológiai élelmiszer vizsgálata
- környezetvédelmi minták vizsgálata
- víztisztító rendszerek és berendezések monitorozása
- diagnosztikai vizsgálatok
- állategészségügyi minták vizsgálata
|
